JACC-BTS 北部战区总医院韩雅玲院士团队揭示Trim55调控心肌梗死后心肌细胞凋亡的作用机制
时间:2024-08-18 15:00:21 热度:37.1℃ 作者:网络
中国心血管病患病率处于持续上升阶段,心血管病死亡仍占城乡居民总死亡原因的首位,其中导致心血管疾病死亡最常见的原因是急性心肌梗死。心肌梗死通常伴随着多种病理改变,其中最严重的是心肌细胞凋亡。然而,临床上尚无针对心肌细胞凋亡的治疗干预策略。因此,寻找预防心肌梗死后心肌细胞凋亡的关键靶点,可为预防和治疗心肌梗死提供新的策略。Trim55是一种心肌和骨骼肌高度表达的E3泛素连接酶,既往研究表明,Trim55在多种心血管疾病中发挥重要作用,包括慢性心力衰竭、糖尿病性心肌病、心肌肥厚和心肌缺血再灌注损伤。然而,Trim55在心肌梗死后心肌损伤中的作用和机制尚未完全阐明。
2024年8月14日,北部战区总医院韩雅玲院士团队在JACC:Basic to Translational Science上发表了题为“TRIM55 aggravates cardiomyocytes apoptosis after myocardial infarction via modulation of Nrf2/HO-1 pathway”的研究论文,初步阐明了Trim55调控心肌梗死后心肌细胞凋亡的具体机制,为心肌梗死的临床防治提供了新的思路和治疗靶点。

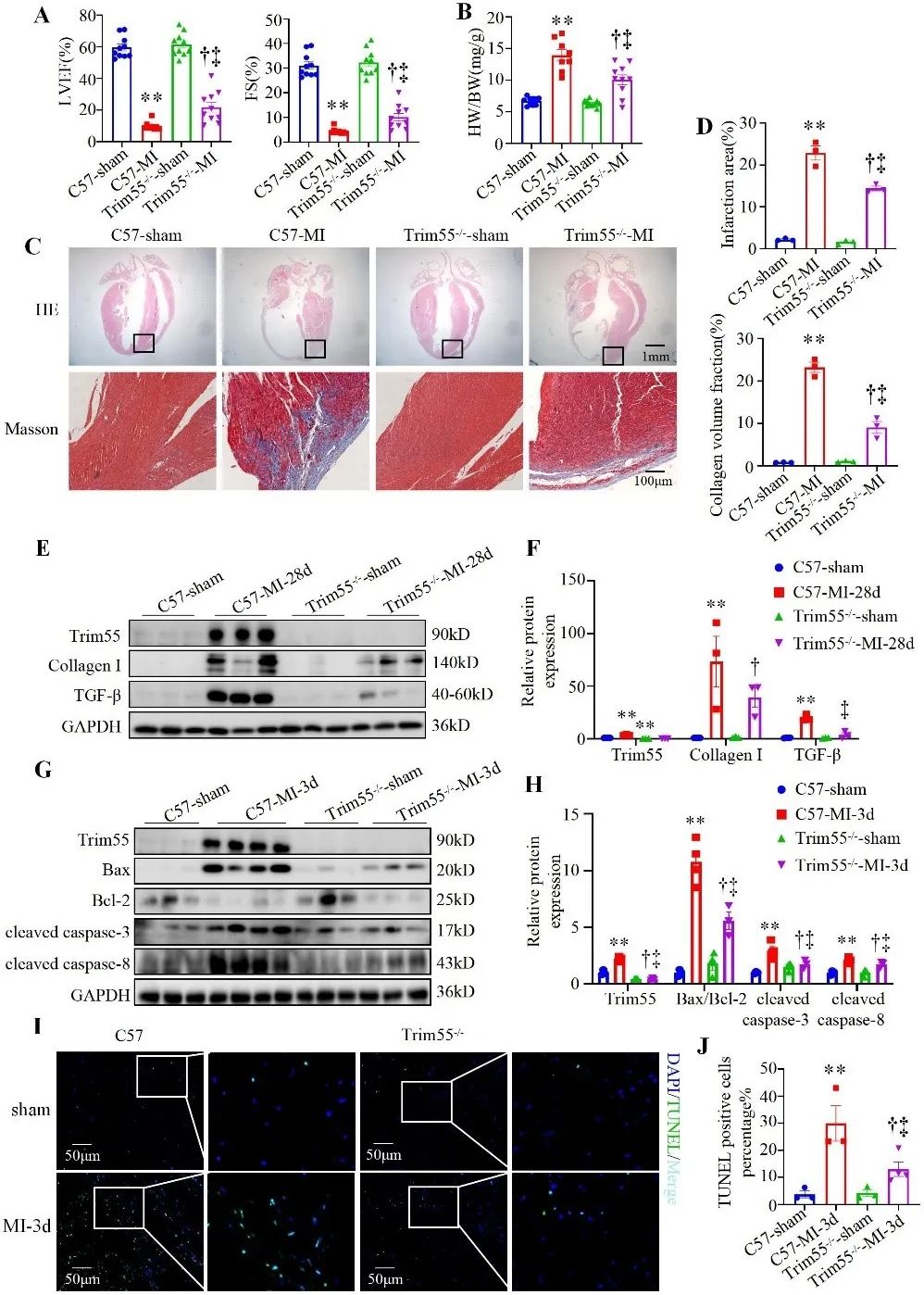
首先,作者采用结扎冠状动脉左前降支的方法构建了小鼠心肌梗死模型,发现心梗后28天,Trim55敲除小鼠的左心室射血分数降低幅度小于对照小鼠,减小了心肌梗死后心室腔的扩大和梗死边缘区的胶原沉积。此外,作者为了进一步探究心功能改善的机制,在心梗3天发现Trim55敲除小鼠的心脏梗死边缘区心肌细胞的凋亡显著减少,提示Trim55敲除对心梗后心肌细胞凋亡具有保护作用。这些研究结果表明,敲除Trim55减少心脏梗死边缘区的心肌细胞凋亡和胶原沉积,改善心功能。
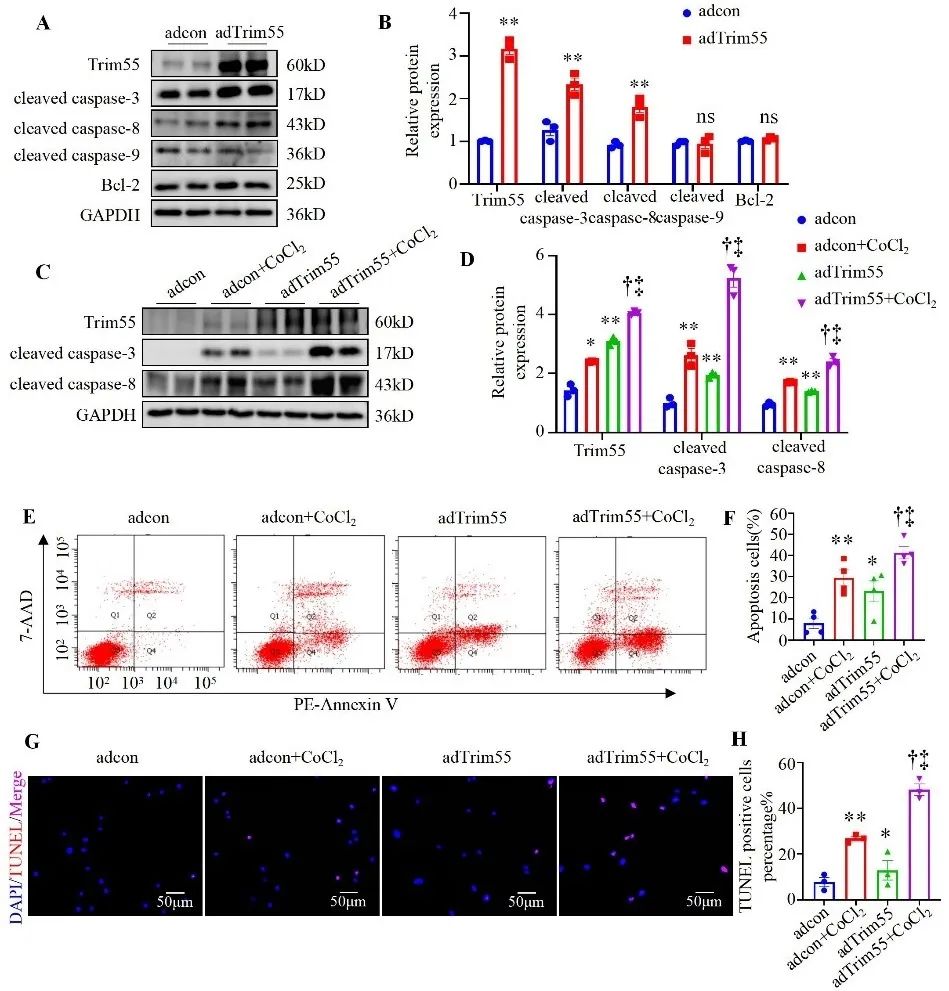
为了阐明Trim55调控心梗后心肌细胞凋亡的具体分子机制,作者采用大鼠原代心肌细胞给予Trim55的腺病毒建立Trim55过表达的细胞,发现Trim55过表达后,心肌细胞凋亡水平显著增加。进一步在Trim55过表达的基础上又给予氯化钴(CoCl2)的缺氧刺激,发现Trim55过表达加重了缺氧引起的心肌细胞凋亡。
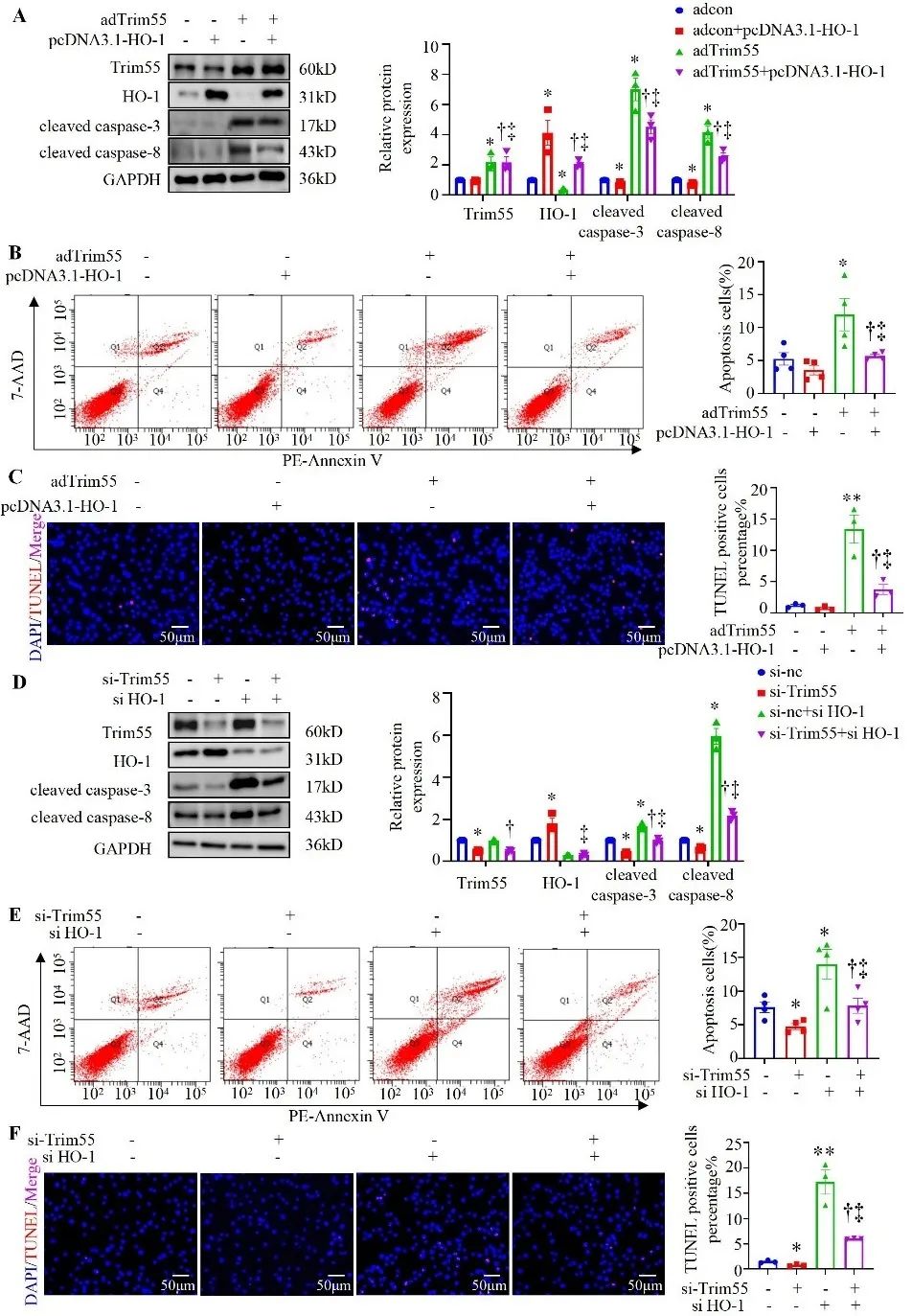
大量研究表明,细胞内活性氧(ROS)的过量产生可导致细胞膜的氧化损伤,从而导致细胞凋亡。因此,作者推测Trim55可能通过调节氧化应激来促进心肌细胞凋亡。已知Nrf2/HO-1通路是一条经典的抗氧化应激通路,作者发现Trim55促进心肌细胞中ROS产生。为了验证Trim55对心肌细胞凋亡的作用是否依赖于氧化应激,在Trim55过表达的基础给予氧化应激通路的下游效应分子HO-1后发现,HO-1过表达可以挽救Trim55过表达引起的心肌细胞凋亡增加,反之, HO-1低表达会使Trim55敲除对心肌细胞凋亡的保护作用消失。此外,作者通过免疫共沉淀实验证明了Trim55与Nrf2之间相互作用,可能是Trim55加速了Nrf2的降解从而抑制了Nrf2/HO-1通路。
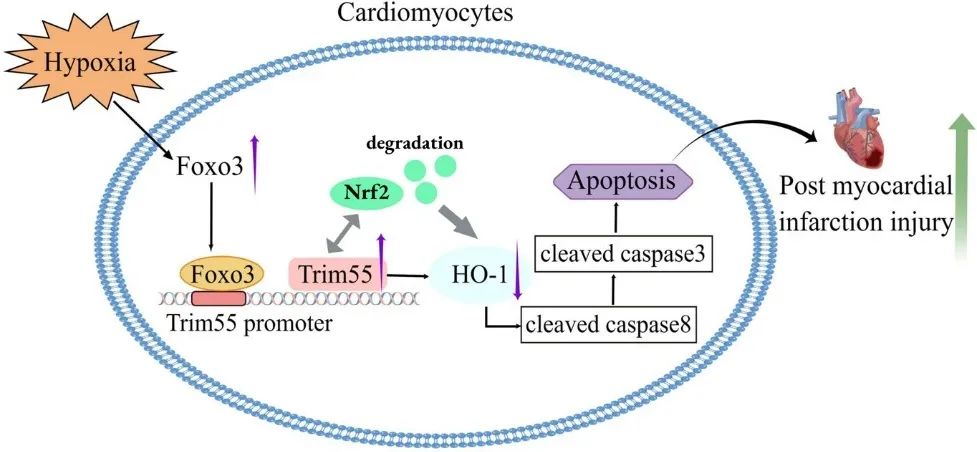
综上所述,该研究初步阐明了Trim55在心肌梗死后心肌细胞凋亡中的重要作用。心肌细胞缺氧后,Foxo3转录激活Trim55使其表达上调,通过抑制Nrf2/HO-1通路促进心肌细胞凋亡,从而加重心肌梗死。这些发现阐明了Trim55在心肌梗死后心肌细胞凋亡中的不利作用,为疾病的防治提供了新的潜在靶点。
该研究由北部战区总医院寒地心血管病全国重点实验室韩雅玲院士团队完成,布雨鑫硕士和刘艳霞主任为本文共同第一作者。该工作得到国家自然科学基金、国家重点研发计划和辽宁省优秀青年基金等项目资助。
原文链接:
https://www.jacc.org/doi/10.1016/j.jacbts.2024.05.006


