指南更新 | 非小细胞肺癌NCCN(2024.V11):新增纳武利尤单抗围手术期治疗方案
时间:2024-10-17 18:00:32 热度:37.1℃ 作者:网络

2024.V11-2024.10.15
非小细胞肺癌
NCCN指南
2024年10月15日,非小细胞肺癌(NSCLC)NCCN指南更新至2024.V11,此次药物治疗更新的主要内容是新增纳武利尤单抗联合含铂双药化疗新辅助治疗,术后纳武利尤单抗辅助治疗无已知EGFR突变或ALK重排的完全切除的Ⅱ-ⅢB期NSCLC患者。详细更新内容如下:
01 更新内容
适合接受免疫检查点抑制剂治疗患者的新辅助全身治疗
🔹“纳武利尤单抗 360 mg联合含铂双药化疗 Q3W 3个周期”修改为“纳武利尤单抗 360 mg联合含铂双药化疗 Q3W 最多4个周期,术后可继续选择纳武利尤单抗单药辅助治疗(对于无已知EGFR突变或ALK重排患者)(1类)”

手术切除后的全身治疗
🔹“帕博利珠单抗 200 mg Q3W或400 mg Q6W 最多一年”修改为“帕博利珠单抗 200 mg Q3W或400 mg Q6W”
针对不同的患者人群对上述帕博利珠单抗方案的使用时长进行了区分:
-
对于无EGFR第19号外显子缺失或第21号外显子L858R突变或ALK重排,且既往接受过辅助化疗,无免疫检查点抑制剂禁忌症的完全切除的ⅡB-ⅢA期、ⅢB期(T3,N2)或高危ⅡA期NSCLC患者,最多使用1年。PD-L1<1%患者的获益尚不清楚
-
对于既往接受过新辅助帕博利珠单抗+化疗的完全切除的Ⅱ-ⅢA期或ⅢB期(T3,N2)NSCLC患者,最多使用39周(1类)
🔹新增“纳武利尤单抗 480 mg Q4W 最多13个周期,用于既往接受过新辅助纳武利尤单抗+化疗且无已知EGFR突变或ALK重排的完全切除的Ⅱ-ⅢB期NSCLC患者(1类)”

02 新增依据
纳武利尤单抗(NIVO)围手术期治疗方案的新增基于一项全球、随机、双盲、Ⅲ期研究(CheckMate 77T研究;NCT04025879),该研究旨在评估“新辅助NIVO+化疗,然后手术和辅助NIVO”的围手术期治疗模式在可切除Ⅱ-ⅢB期NSCLC患者中的疗效和安全性。
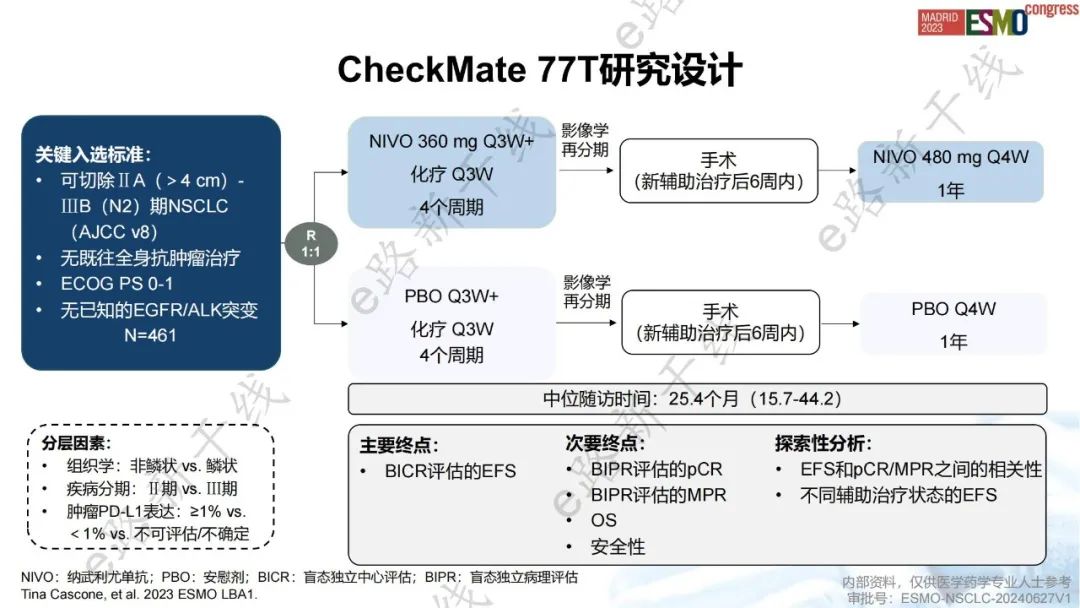
研究设计图
2023 ESMO年会报告了EFS的期中分析结果1,研究结果显示,中位随访25.4个月,在可切除NSCLC患者中,NIVO+化疗/NIVO组与化疗/安慰剂(PBO)组相比,主要终点EFS的改善具有统计学意义和临床意义(中位数:NR vs. 18.4个月;HR,0.58;P=0.00025)。pCR率(25.3% vs. 4.7%)和MPR率(35.4% vs. 12.1%)也得到改善。
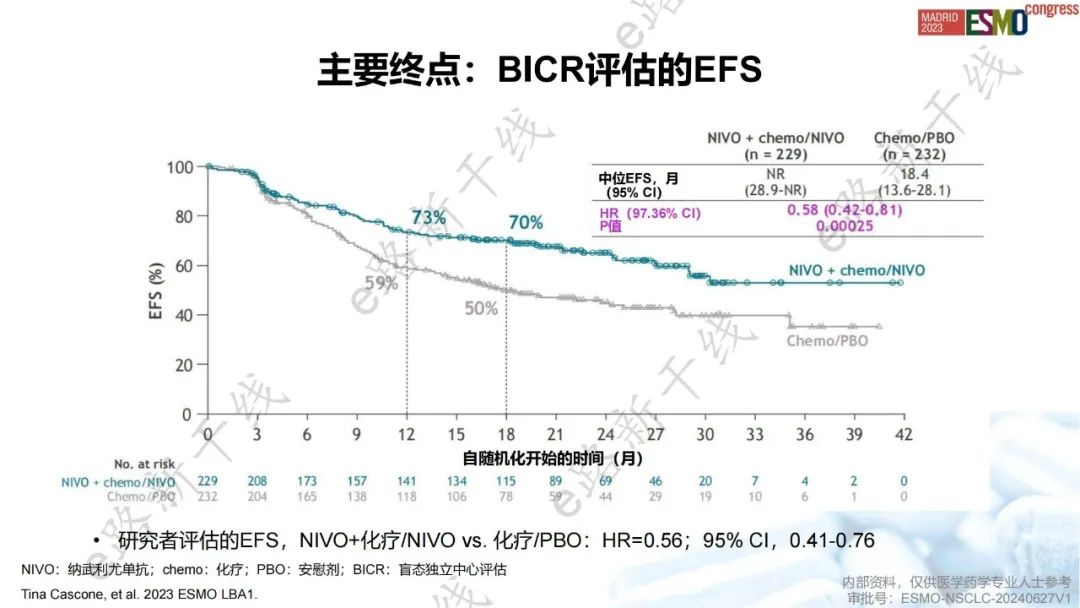
EFS结果(中位随访时间:25.4个月)
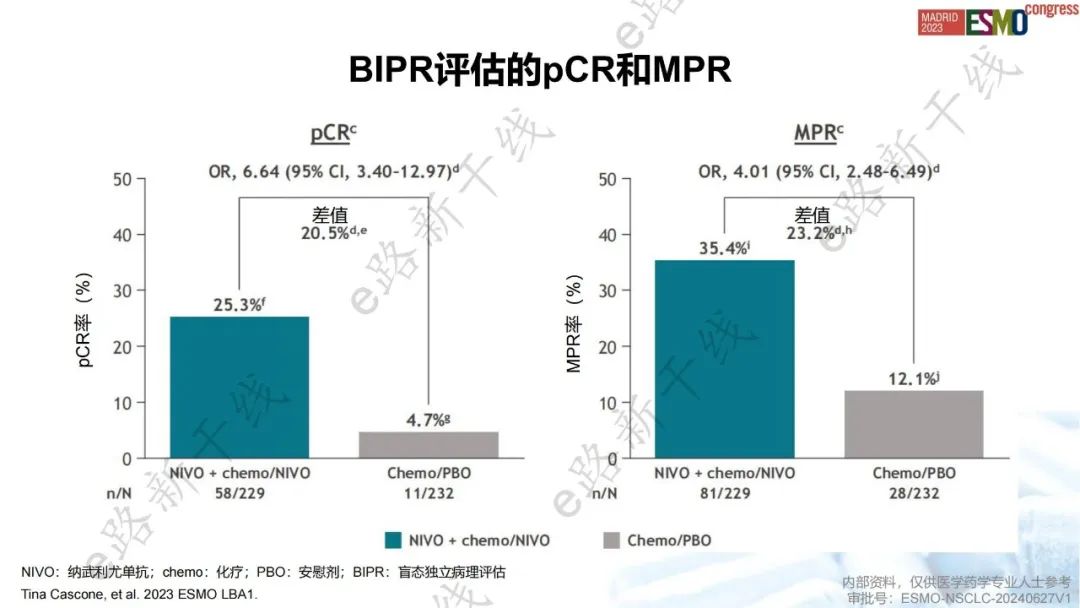
pCR和MPR结果
安全性方面,NIVO+化疗/NIVO组和化疗/PBO组任何等级AE的发生率分别为97% vs. 98%(3/4级:47% vs. 43%);两组任何等级TRAE的发生率分别为89% vs. 87%(3/4级:32% vs. 25%)。总体安全性可控,未发现新的安全性信号。
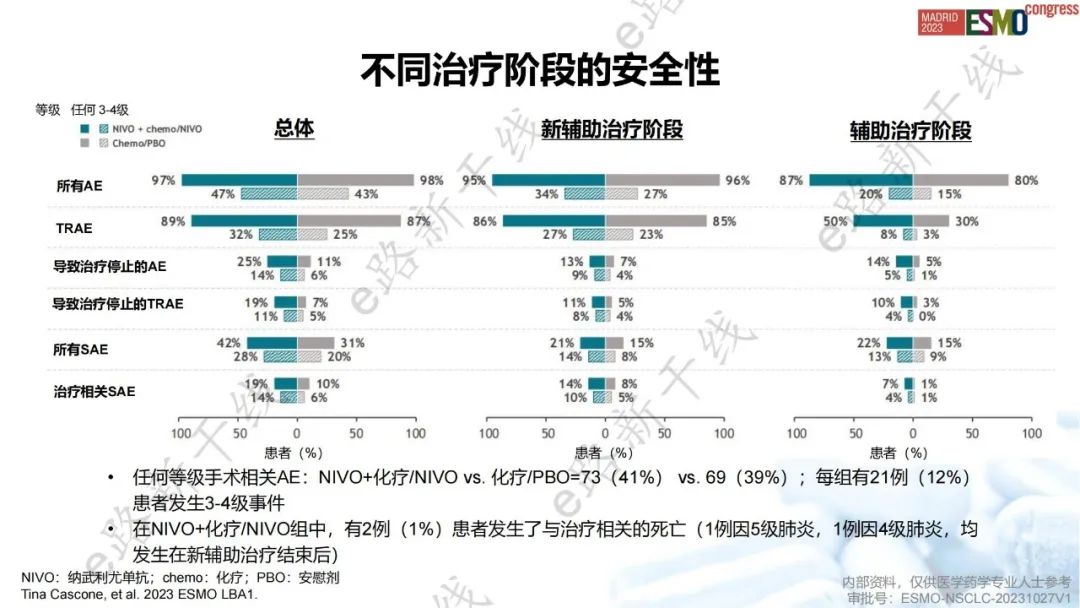
安全性结果
2024 ESMO年会报告了该研究中位随访33.3个月后的结果2,更新分析显示,在可切除NSCLC患者中,围手术期NIVO相比于PBO继续显示出EFS获益(中位数:40.1个月 vs. 17.0个月;HR,0.59)。
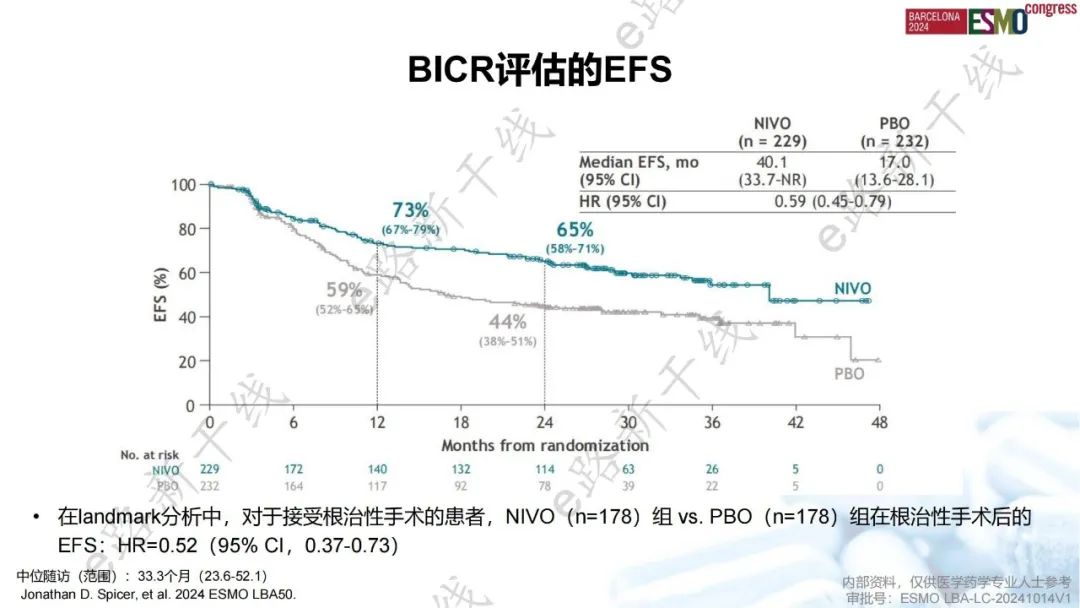
EFS更新结果(中位随访时间:33.3个月)
2024年10月3日,基于CheckMate 77T研究的积极结果,FDA批准了纳武利尤单抗联合含铂双药化疗新辅助治疗,术后纳武利尤单抗单药辅助治疗无已知EFGR突变或ALK重排的可切除(肿瘤≥4 cm和/或淋巴结阳性)NSCLC成人患者。
FDA关于新辅助/辅助纳武利尤单抗治疗可切除NSCLC获批的公告
03 总结
NSCLC围手术期治疗已全面进入免疫治疗时代,多项Ⅲ期临床研究证实新辅助ICI联合化疗+辅助ICI治疗能够显著提高可切除Ⅱ-Ⅲ期NSCLC的生存获益,成为了Ⅱ-Ⅲ期NSCLC围手术期治疗新标准,CheckMate 77T研究的成功为该治疗模式再添新证据。
参考文献:
1.Tina Cascone, et al. 2023 ESMO LBA1.
2.Jonathan D. Spicer, et al. 2024 ESMO LBA50.
3.NCCN指南:非小细胞肺癌(2024.V11).


